预约小初高体验课 享受1对1辅导
各位家长请注意:此表单用于预约体验课,不想预约的家长,请勿填写
| 高一衔接 | 2021高一高二开学资料领取[ 戳我下载 ] |
| 高中资料 | 2021及历年高一期末高二期末试卷真题及答案[ 戳我下载 ] |
| 【新高考福利】备考规划+全科复习资料[ 戳我下载 ] |
原电池电极判断及相关现象分析,“电化学”板块是化学高考中的可能会考内容,多以选择题形式出现,亦或参杂在后边的解答题中一起考察,考察分数为6——8分。所以“电化学”的学习,一直是高中化学的重点内容。学而思1对1小编为大家整理了原电池电极判断及相关现象分析,希望对大家有所帮助。
原电池电极判断及相关现象分析
一、构成原电池的基本条件

1、活泼型不同的两个电极
2、可以自发进行氧化还原反应
3、形成闭合回路
4、有电解质溶液
二、原电池电极极性的判断
1、根据电极材料判断
一般情况下,活泼性强的金属为负极,活泼性较弱的金属或导电的非金属为正极。
2、根据电极反应类型判断
失去电子发生氧化反应的电极为负极,得到电子发生还原反应的电极为正极。
3、根据电极反应现象判断
参与电极反应不断溶解的电极为负极(燃料电池除外);质量增加或附近有气泡产生的电极为正极。
4、根据电子流动方向(或电流方向)判断
在外电路中,电子由原电池的负极流向正极,电流由原电池的正极流向负极。
5、根据电解质溶液中离子流动方向判断
在内电路中,阳离子向正极移动,阴离子向负极移动。
6、根据电池总反应式判断
若给出电池总反应式,通过标出电子转移的方向可知,失去电子的一极为负极,得到电子的一极为正极。
7、误区
原电池负极的判断,不能一味的根据金属活动性顺序来判断,而是应理解为“较易与电解质溶液反应的电极是原电池的负极”。
例如,Mg、Al为两极,NaOH溶液为电解质溶液时,Al能与NaOH溶液反应,而Mg不能与NaOH溶液反应,虽然Al较Mg不活泼,但Al却作该原电池的负极。
光看不练假把式!
题型一:原电池电极极性及现象判断
【例题】将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,下列叙述正确的是
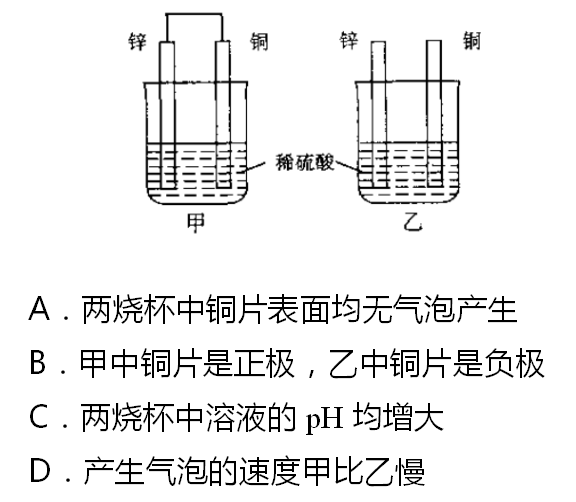
【解析】甲装置为原电池,因为锌的金属性更活泼,所以锌电极为负极,铜电极为正极。故负极Zn失电子,正极H+得电子,有气泡产生,且溶液pH增大。
乙装置没有形成闭合回路,故乙装置不构成原电池,仅为金属锌和稀硫酸的反应;铜电极表面没有气泡产生。因为锌与稀硫酸反应,消耗了H+,所以溶液pH增大。
综上所述,A、B均错误,C正确。
又因为形成原电池可以加快反应速率,所以甲装置产生气泡的速度比乙快,故D错误。
【训练】
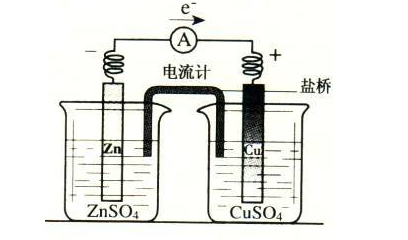
有关如右图所示原电池的叙述,正确的是(盐桥中装有含琼胶的KCl饱和溶液)
A、铜片上有气泡逸出
B、取出盐桥后,电流计依然发生偏转
C、反应中,盐桥中的K+会移向CuSO4溶液
D、反应前后铜片质量不改变
氢:尽管小到卑微,我也会倾尽全力,还原你的本质。
【解析】因为锌的金属性大于铜,所以锌为负极,铜做正极。负极Zn失电子形成Zn2+,正极溶液中的Cu2+得电子形成铜单质,附着在铜电极表面。故铜电极表面没有气体溢出,A错误;取出盐桥后原电池不构成闭合回路,反应无法进行,故没有电流流过,B错误;反应过程中,阳离子移向正极,故Cu2+移向CuSO4溶液,C正确;反应过程中有Cu析出,故Cu电极质量增加,D错误。
题型二:根据电极现象,判断金属活动性
【例题】把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,电流由d到c;a、c相连时,c极上产生大量气泡;b、d相连时,b上有大量气泡产生,则四种金属的活动性顺序由强到弱为()
A、a>b>c>d
B、a>c>d>b
C、c>a>b。>d
D、b>d>c>a
【解析】若a、b相连时,a为负极,则说明金属性:a>b;
若c、d相连时,电流由d到c,则说明金属性:c>d;
若a、c相连时,c极上产生大量气泡,则说明金属性:a>c;
若b、d相连时,b上有大量气泡产生,则说明金属性:d>b;
综上所述:金属性顺序为a>c>d>b,故选B。
【训练】
X、Y、Z、M代表四种金属元素,金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;金属Y和Z用导线连接放入含Y2+的溶液中时,Y在Y极上析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为()
A、X>Z>Y>M
B、X>Y>Z>M
C、M>Z>X>Y
D、X>Z>M>Y
氢:尽管小到卑微,我也会倾尽全力,还原你的本质。
【解析】若金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出,则说明金属性:X>Z;
若金属Y和Z用导线连接放入含Y2+的溶液中时,Y在Y极上析出,则说明金属性:Z>Y;
若M2+的氧化性强于Y2+,则说明金属性:Y>M;
综上所述:金属性顺序为X>Z>Y>M,故选B。
原电池电极判断及相关现象分析已经为大家整理好了。感谢您的阅读。如果大家想咨询学而思1对1课程和8人班小组课程,可以拨打4000-121-121。如果大家想一起探讨学习和诊断欢迎大家加入智康QQ群,里面有老师为你解答。小学②群:213965478、中考家长交流①群:230753443、高中交流群:228799125还可以微信搜索“成都学而思1对1”微信号:cdxrs1d1,更多学习资料等你下载!
 请加入QQ群,试题资料免费放送!
请加入QQ群,试题资料免费放送!

 保存 |
保存 |
 打印 |
打印 |
 关闭
关闭
